
私たちの研究はどのように終わるのだろうか 。GMOサーモン
に関する過去のトピック は、ハブラキターにとって非常にうまくいっているようです。植物の改変に関する資料を準備している間、同様に興味深いトピックであるホモサピエンスの遺伝子改変を検討することをお勧めします。これは非常に物議を醸すホリバートピックであり、無視することはできません。 私はすぐに物議を醸すように見えるかもしれないが、科学界でどういうわけか解決される必要があるいくつかの論文を与えるでしょう:
- 私たちは退化しています。毎年、弱い人が生き残り、子供を産み、遺伝子プールに負担をかけます。修正する必要があります。
- 単純な禁止は役に立ちません。たとえば、ヨーロッパで実験が禁止されている場合、中国が実験を行います。
- 私たちは遺伝病の治療にとどまりません。遅かれ早かれ、軍隊は彼らの超兵士や青い目をしたより強くて賢い子供たちを望んでいる人々と一緒になります。
私は、人々の遺伝子型への介入の既存の技術の概要を説明すると同時に、それが私たちを脅かしているものを分析します。
遺伝子治療とは
まず、用語を定義しましょう。遺伝子治療は、特定の病気を治療することを目的としたヒトゲノムへの介入です。さらに、介入は体細胞にのみ行われます。これらは生殖しない細胞です。明らかに、新世代の突然変異やバグ修正を修正する必要はありません。今のところ、少なくとも。
実際の動物実験は1980年代頃に始まりましたが、それは臆病なステップにすぎませんでした。真核生物のベクターを表現するDNAプリンターのような美しさはありませんでした。
どこに本当に介入できますか?
プラスミド
まず、基本的な遺伝情報が含まれている細胞核を離れることができます。プラスミドを使用できます。

1)細菌の染色体DNA 2)プラスミド
プラスミドはほとんど細菌性です。原始的な菌類やいくつかの植物に時々見られます。実際、これはDNAですが、リングに折りたたまれ、細胞質に別々に浮かんでいます。つまり、遺伝物質を保存するためのそのような別個のメカニズム。バクテリアにとって、それらは、例えば、抗生物質保護オプションについて「隣人に伝える」ために、陽性の突然変異を伝達するために非常に重要です。プラスミドをヒトに使用する際の秘訣は、細胞に導入されてからしばらくすると、プラスミドが自然に崩壊することです。そしてそれらはまた細胞の主要な遺伝的装置に影響を与えません。つまり、メインファームウェアは影響を受けません。
カーネルへのパッチ適用
次に、カーネル内のコードスニペットを直接編集する機能があります。これはより侵襲的な手順であり、すでにDNAの一部を不正確に挿入または切り取るリスクがあります。しかし、体細胞は分裂し、パッチを当てたバージョンのDNAを子孫に伝達するため、これは実際にはいくつかの深刻な遺伝的欠陥を根本的に修正する唯一のオプションです。
ミトコンドリア
ミトコンドリアは細胞内の原子炉のようなものです。それらは脂肪酸とブドウ糖を消費し、出口でそれらはマクロエルグ(高い結合エネルギーを持つ物質)をスタンプします。たとえば、ATP。これは、すべてのアクティブな反応、たとえば、濃度勾配に対する浸透圧膜ポンプの操作のための普遍的な「燃料」です。
彼らには特異性があります-彼ら自身の遺伝的装置です。実際、これらはまさにこの理由から、半自律的なシンビオントのように見えます。彼らの遺伝的装置は、ミトコンドリアDNAの先天性突然変異で支配するのが理にかなっています。通常、これらは非常に重度の先天性症候群でもあります。
ウイルスベクターは注射器のようなものです
最初の重要なポイントは、配信ツールであるウイルスベクターの開発です。哺乳類のための最初のそのようなウイルスは1984年に 開発されました。マウスレトロウイルスを分子注射器として使用した。彼はそれ自体が非常に不快な道具でした。なぜなら、それは高い確率で腫瘍性疾患を引き起こしたからです。実際、その2番目の名前はマウス白血病ウイルス(MLV)です。将来的には、開発はより安全なオプションに切り替わりました。
ウイルスベクターとは正確には何ですか?これは、1回だけ機能する特別に変更されたウイルスです。注射器のように。これを行うには、彼はいくつかの基準を満たす必要があります。
セキュリティ
ウイルスベクターは自発的に増殖できないはずです。このために、彼らはビルトインキルスイッチを持っています。それらのゲノムは最初は非常に損傷しているため、自律的に複製することはできません。実験室環境では、それらは、かけがえのない成分と、組み立てに必要なタンパク質の一部を生成する追加の補助ウイルスの存在下でのみ、細胞培養で増殖します。つまり、それは実験室の培養フラスコで増殖しますが、体内では一度機能し、細胞を半組み立てされた形で残して死にます。
低い細胞毒性
多くのウイルスは宿主細胞にとって非常に残酷です。潜伏期の後、細胞は枯渇により死に、新しいビリオンはその死すべき遺物から全方向に散乱します。同時に、寄生する細胞の正常な生理機能に特に影響を与えないウイルスもあります。たとえば、アデノウイルス。
安定
ウイルスは遺伝的に安定している必要があります。たとえば、インフルエンザは機能しません。彼には「パリティ」のわかりやすいメカニズムがなく、コピー後のハッシュが収束しなかったことを気にしません。これが彼の進化戦略です。それどころか、同じコロナウイルスには制御と修復のメカニズムがあり、遺伝物質の安定性が高まります。他の理由でベクターとして使用されていませんが。したがって、タスクは、バイオリアクターでの複製の過程でウイルスが同じペイロードを保持することを保証することです-ペイロードは変更されません。
細胞型特異性
ウイルスは、その負荷をどこにでも配信するだけでなく、特定の種類のセルに正確に配信する必要があります。これは、欠陥のある赤血球に関連する病気を治療する必要がある場合、ウイルスは血球の多能性前駆幹細胞に非常に正確に感染する必要があることを意味します。同時に、筋肉組織などを引っ掛けないでください。
遺伝子治療に関してすでに行われていること
最初のヒトの遺伝的矯正は1990年に実施されました。4歳のアシャンティデシルバは、ADA酵素の欠損に関連する複雑な複合免疫不全の重症遺伝子欠損の治療を受けました。編集されたのはTリンパ球を産生する幹細胞のゲノムではなく、彼女自身のドナー血液からの成人T細胞であったことに注意する必要があります。つまり、彼女は将来これらの手順を繰り返す必要がありました。次に、同様の技術を使用してSCID(重症複合免疫不全症)を治療するための一連の成功した実験プロトコルがありました。
1999年に、この分野の研究を大幅に遅らせる事件が発生しました。ジェシー・ゲルシンガーは、アンモニアを解毒することができなかったために遺伝性肝疾患に苦しんでいました。遺伝子の健康なコピーを含むアデノウイルスベクターの導入から4日後、彼は過免疫反応と多臓器不全の結果として死亡した。その後、FDAは、研究プロトコルに多数の違反があったと結論付けました。
2006年に、腫瘍学の治療のための成功した個々の遺伝子治療プロトコルの最初の報告が現れました。キラーT細胞は特定の種類の腫瘍用にプログラムされており、患者の体内に放出されます。
2011年に認められた HIV療法2008年に患者ゲロヒュッターで。この方法は、骨髄を完全に除去してから、CCR5受容体を無効にする二重のdelta-32変異を持つ修正された細胞を移植する必要があるため、特に幅広い対象者に適用できません。
2013年までに、世界で認可された遺伝子薬は5つだけでした。腫瘍学からの3つ、遺伝性リポタンパク質リパーゼ欠損症および新血管原の治療のためのグリベラ。ちなみに後者は完全に私たちが開発したものです。
ネオバスカルゲン
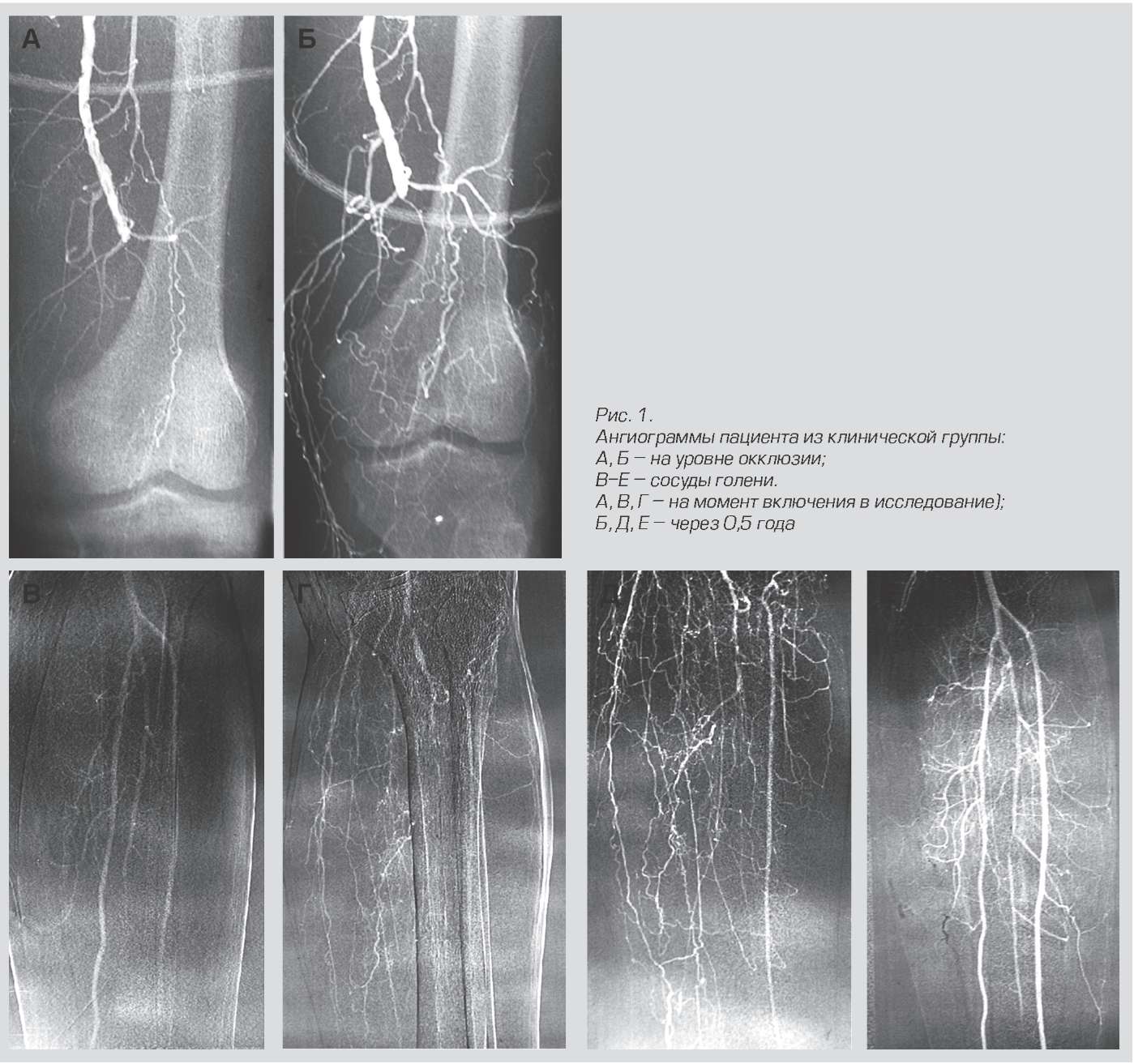
Neovasculgenによる治療の結果。
この薬はプラスミドに属しています。つまり、細胞自体のゲノムを編集するのではなく、限られた時間だけ機能するプラスミドをプラスミドに送達するだけです。
(), VEGF 165, (VEGF — Vascular Endothelial Growth Factor). , . , , .
ヒト幹細胞研究所
作用機序は興味深いものです。注射部位の細胞は、血管増殖因子であるVEGFの合成を開始します。その結果、新しい分岐毛細血管ネットワークがこの領域で成長し始めます。これは、たとえば糖尿病やアテローム性動脈硬化症による慢性下肢虚血の患者にとって重要です。この薬の前に、より多くの切断がありました。現在では、インプラントの生着のための歯科での使用についてもテストされています。遺伝子調製物は骨材料と混合され、縫合されます。その結果、血管は急速に成長し、必要な組織が拒絶されることなく形成されます。ウサギは頭蓋骨の断片の移植中にすでに正確にシミュレートされています。私の知る限り、次は人です。
ゾルゲンスマ
脊髄性筋萎縮症は非常に厳しい病気であり、ホーキングが受けた筋萎縮性側索硬化症と臨床的にいくらか似ていますが、他の原因もあります。病気の進行の結果として、麻痺が進行し、呼吸ができないために死に至ります。
ゾルゲンスマは、脊髄性筋萎縮症の最初の遺伝子治療薬です。AveXis(ノバルティス)が制作。SMN遺伝子の作業コピーは、血液脳関門を通過して患者の細胞に入ることができるアデノ随伴ウイルス(AAV)血清型9、AAV9を使用して注入されます。1つの問題-それは絶対に莫大なお金がかかります。1回の注射の費用は210万ドル(約1億5200万ルーブル)を超えます。しかし、結果も素晴らしいです。人間の場合、運動機能は回復し、病気はそれ以上進行しません。理論的には、そのような高価な操作は国によって支払われるべきです。個人にとって、希少疾患の治療費は法外なものです。
次は何ですか?
ここに非常に難しい質問があります。私たちは集団に欠陥遺伝子を蓄積します。以前は、心臓の欠陥を持つ子供は単に死ぬでしょう-今、彼らは彼を救い、彼はこの欠陥を持つ子孫を与えるでしょう。以前は、多くの妊娠が長続きしませんでした。現在、妊娠中の女性は流産の割合を最小限に抑えて引き抜かれ、正常な出産で完了しています。実際、私たちは自然集団の淘汰のメカニズムを打ち破っています。これは正しくて人道的ですが、遺伝子プールの蓄積された突然変異で何かをしなければなりません。
グリーンカードと繁殖許可を取得するか、遺伝的異常を確実かつ安全に修正する方法を学びます。近視、全身性結合組織異形成、および他の多くの先天性欠損症を捨てるのはクールでしょう。そして最後に、すべての正常な哺乳類のように、ブドウ糖からのビタミンCの合成に関与するその愚かな壊れた遺伝子を修正します。
ここでは、未知の未来だけが私たちをさらに待っています。最も憂慮すべきは、人口の最も裕福なセグメントが子供たちを糖尿病、アテローム性動脈硬化症から解放するように変更し、同時に少しのミオスタチンを粉砕して、多くの努力なしに運動しているように見せることで、社会の潜在的な層別化です。涼しい。しかし、それは怖いです。
